| 发现之旅 |  |
| 深入思考 |  |
将左右两个小球调换位置,然后再分别放入热水和冰水中,观察两个小球的颜色变化。
 |
 |
|
由此可以得出一个结论:在其他条件不变的情况下,温度升高,会使化学平衡向着吸热反应方向移动,温度降低,会使化学平衡向放热反应方向移动。
用注射器吸入少量NO2和N2O4的混合气体,然后将注射器针头插入橡皮塞中以封口。将注射器活塞反复往里推和往外拉,观察注射器中气体颜色的变化。
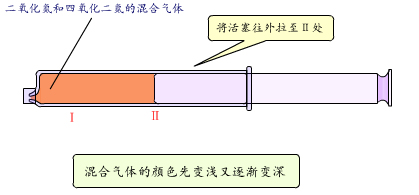
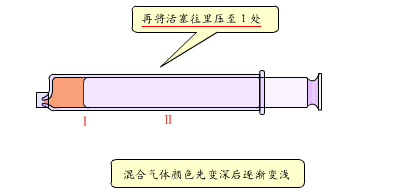
这些变化应该怎么解释呢?其实是由于针筒内体积增大,使气体的压强减小,浓度也减小,颜色变浅。后来颜色逐渐变深,这必然是由于化学平衡向着生成NO2反应的方向即气体体积增大的方向移动了。当活塞往里推时,混合气体的颜色先变深又逐渐变浅。这必然是由于针筒内体积减小,气体的压强增大,浓度也增大,颜色变深。由于化学平衡向着生成N2O4的方向即气体体积缩小的方向移动,因此混合气体的颜色又逐渐变浅了。
由此可以得出结论:在其他条件不变的情况下,增大压强,会使化学平衡向着气体体积缩小的方向移动;减小压强,会使化学平衡向着气体体积增大的方向移动。
注意:在有些可逆反应里,反应前后气态物质的总体积没有变化,或者没有气体参加反应或气体生成,在这两中情况下,增大或减小压强都不能使化学平衡移动。
(三)由于催化剂能够同等程度地增加正反应速率和逆反应速率,因此它对化学平衡的移动没有影响。也就是说,催化剂不能改变达到化学平衡状态的反应混合物的组成,但是使用催化剂,能够改变反应达到平衡所需的时间。
| 学有所用 |  |
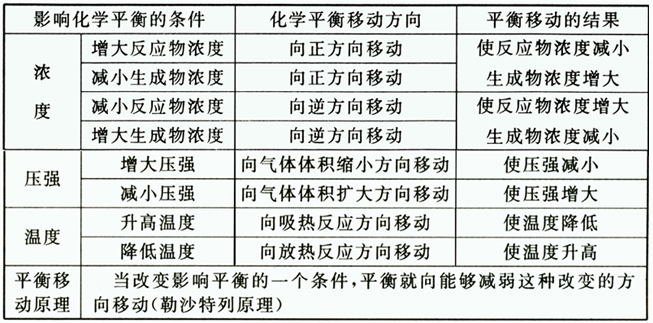
影响化学平衡的因素规律
| 沙场练兵 |  |
1.在一个固定体积的密闭容器中,放入3LX气体和2LY气体,在一定条件下发生下列反应![]() 达到平衡后,容器内温度不变,混合气体的压强比原来增加5%,X的浓度减小
达到平衡后,容器内温度不变,混合气体的压强比原来增加5%,X的浓度减小![]() ,则该反应方程式中的 n 值是( )
,则该反应方程式中的 n 值是( )
A. 3 B. 4 C. 5 D.6
2.在密闭容器中,存在下列平衡:![]() 温度不变时,增加N2O4的浓度,当建立新的平衡后,
温度不变时,增加N2O4的浓度,当建立新的平衡后,
(1)平衡常数的值与原来相比较将是( )
A.变大
B.变小
C.不变
D.不好比较
(2)新平衡时的c(N2O4)与原平衡的c(N2O4)相比将( )
A.变大 B.变小 C.不变 D.缺少数据,无法比较
3.将固体NH4I置于密闭容中,在某温度下发生下列反应:![]() 当反应达到平衡时,[H2]=0.5mol/L,[HI]=4mol/L,则NH3的浓度为 ( )
当反应达到平衡时,[H2]=0.5mol/L,[HI]=4mol/L,则NH3的浓度为 ( )
A.3.5mol/L B.4.0mol/L C.4.5mol/L D.5.0mol/L
4.在一定条件下的某可逆反应:![]() ,反应达到化学平衡的体现是( )
,反应达到化学平衡的体现是( )
A.单位时间内生成2n mol A同时生成n mol D
B.容器内压强不随时间而变化
C.容器内混合气体的密度不随时间而变化
D.单位时间内生成n mol B,同时消耗1.5 n mol C
5.![]() (正反应为吸热反应)的可逆反应中,在恒温条件下,B的体积分数B%与压强(P)关系如图所示。有关叙述正确的是( )
(正反应为吸热反应)的可逆反应中,在恒温条件下,B的体积分数B%与压强(P)关系如图所示。有关叙述正确的是( )


6.二氧化氮能形成二聚分子:![]() 。现欲测定二氧化氮的相对分子质量,应采用的适宜条件为( )
。现欲测定二氧化氮的相对分子质量,应采用的适宜条件为( )
A.高温低压
B.低温高压
C.低温低压 D.高温高压
7.密闭容器中一定量的混合气体发生反应:![]() ,平衡时,测得A的浓度为0.50mol・L-1,在温度不变时,把容器容积扩大到原来的2倍,使其重新达到平衡,A的浓度为0.30mol・L-1,有关叙述不正确的是( )
,平衡时,测得A的浓度为0.50mol・L-1,在温度不变时,把容器容积扩大到原来的2倍,使其重新达到平衡,A的浓度为0.30mol・L-1,有关叙述不正确的是( )
A.平衡一定向右移动 B.B的转化率降低
C.![]() D.C的体积分数降低
D.C的体积分数降低

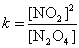 ),而k不变,新平衡的c(N2O4)大于原平衡的c(N2O4)
),而k不变,新平衡的c(N2O4)大于原平衡的c(N2O4)