| 发现之旅 |  |
| 深入思考 |  |
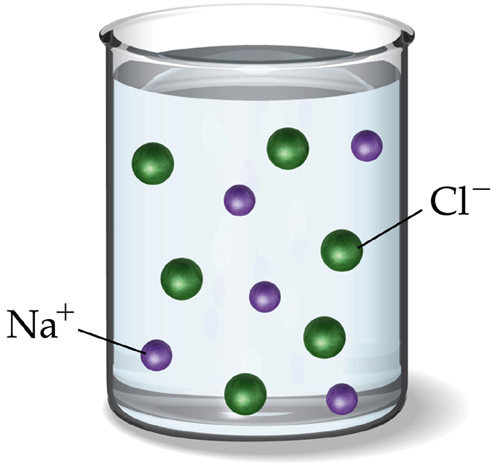

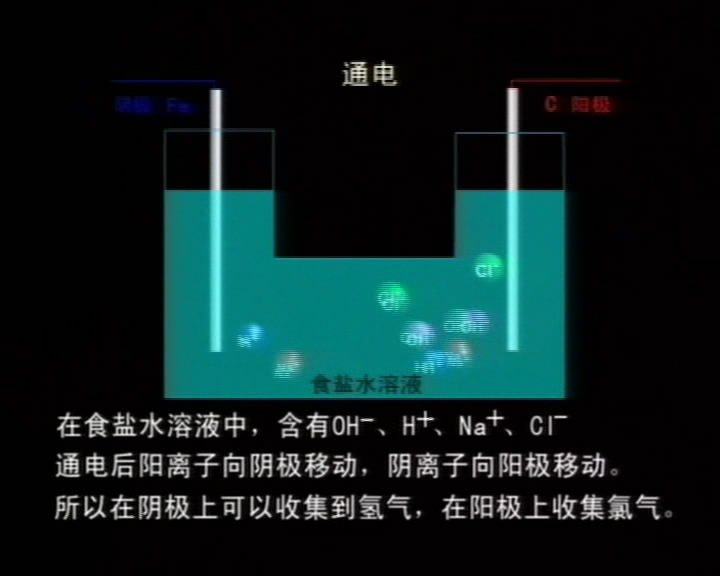
当接通直流电源后,带负电的OH-和Cl-向阳极移动,带正电的Na+和H+向阴极移动。当接通直流电原后,带负电的OH-和Cl-移向阳极,带正电的Na+和H+移向阴极。在这样的电解条件下,在阳极,Cl-比OH-容易失去电子被氧化成氯原子,氯原子两两结合成氯分子放出。
2Cl-2e====Cl2↑ (氧化反应)
2H++2e====H2 (还原反应)
2NaCl+2H2O 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
| 学有所用 |  |
离子交换膜法制烧碱
点击上图观看“离子交换膜法电解原理”视频

离子交换膜法电解制碱的主要生产流程
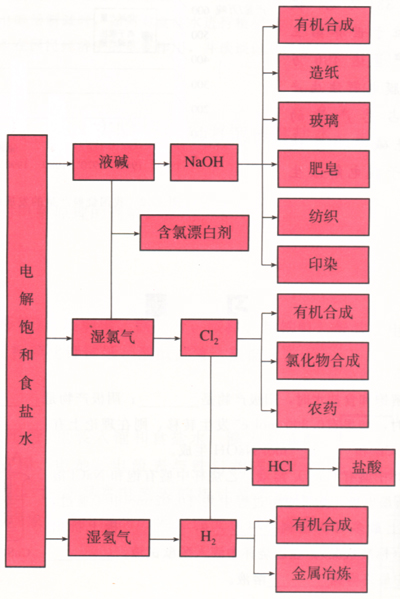

氯碱工业产品
| 沙场练兵 |  |
1. 图中能验证氯化钠溶液(含酚酞)电解产物的装置是( )
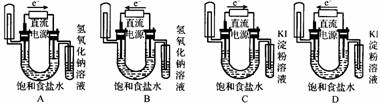
2. 将一直流电源的正、负极,分别连通在一张用食盐水、碘化钾、淀粉溶液和石蕊溶液浸透的滤纸上,经过一段时间后,两极附近滤纸的颜色分别是( )
A |
B |
C |
D |
|
阳极 |
蓝 |
百 |
红 |
蓝 |
阴极 |
百 |
蓝 |
蓝 |
蓝 |
3. 某同学想制作一种家用环保型消毒液发生器,用石墨做电极电解饱和氯化钠溶液,通电时,为使![]() 被完全吸收制得有较强杀菌能力的消毒液,设计了如图的装置,则对电源电极名称和消毒液的主要成分判断正确的是( )
被完全吸收制得有较强杀菌能力的消毒液,设计了如图的装置,则对电源电极名称和消毒液的主要成分判断正确的是( )
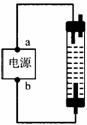
A.a为正极,b为负极;NaClO和NaCl
B.a为负极,b为正极;NaClO和NaCl
C.a为阳极,b为阴极;HClO和NaCl
D.a为阴极,b为阳极;HClO和NaCl
4. 实验室用铅蓄电池电解食盐水制取氯气,已知铅蓄电池放电时发生的反应为负被,![]() 正极:
正极:![]() 。当制得
。当制得![]() 0.05mol时,电池内消耗硫酸的物质的量至少是( )
0.05mol时,电池内消耗硫酸的物质的量至少是( )
A.0.025mol B.0.050mol C.0.10mol D.0.20mol