| 发现之旅 |  |

| 深入思考 |  |

硫酸生产厂
 |
 |
黄铁矿 |
石膏 |
其中造气是在沸腾炉中进行的,将粉碎过的黄铁矿放在沸腾炉中燃烧,从而得到有用的炉气。用黄铁矿制得的炉气含有SO2、O2、N2、水蒸气以及一些杂质,所以在进入接触室时要进行净化和干燥处理。炉底通入氢气的作用是把炉内的矿粒吹得剧烈翻腾,好象沸腾着的液体,使矿粒能充分燃烧。

化学反应方程式 |
|
热化学反应方程式 |
 |
接触氧化是在接触室中进行的,从沸腾炉中出来的经过净化和干燥的炉气(其成分体积分别约为:SO27%、O211%、N282%)进入接触室发生氧化反应,生成SO3。
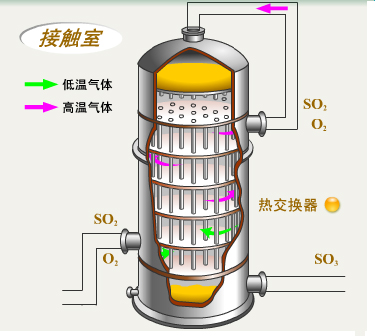
化学反应方程式 |
|
热化学反应方程式 |
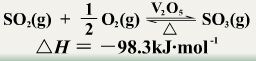 |
化学反应方程式 |
|
热化学反应方程式 |
| 学有所用 |  |
硫酸在工业中的用途
硫酸大量用于清洗钢铁的表面。在钢铁进行冷轧、冷拔和冲压等加工之前,必须清除钢铁表面的氧化铁,否则,在冷轧、冷拔和冲压时氧化铁就可能被压入钢铁中,使钢铁的表面很粗糙,甚至造成废品。氧化铁的存在也会使轧辊或冲模等工具很快被磨损。在金属表面镀镍或镀铬时,也要用硫酸清洗金属表面,否则镀层很容易脱落下来。
硫酸还是生产化肥的原料。把氨通入 75% 硫酸中,可以生成硫酸铵。这个反应放出大量的热,这些热量用来将水分蒸发,便可得到硫酸铵晶体。硫酸铵和尿素都是重要的氮肥。硫酸也是生产过磷酸钙肥料的原料。
在石油精炼中,要用浓硫酸除去汽油和润滑油中的杂质 ―― 硫化物和不饱和碳氢化合物,每精炼 1t 石油要用 24kg 浓硫酸。
在有机化工中,硫酸是生产农药敌百虫、以及合成洗涤剂烷基苯磺酸钠的原料。很多基本有机化工原料如甲酸、草酸、柠檬酸、苯酚、乙酸乙酯也要用硫酸做原料。
在无机化工生产中,硫酸用于生产氢氟酸、铬酸、磷酸、硫酸铜、硫酸铝、硫酸锌、硫酸镍以及钛白粉、立德粉等颜料。
总而言之,在肥料、冶金、石油精炼、农药、炸药、纺织、染料、塑料、油漆、电池、制革、颜料、药品和洗涤剂等工业中,处处都离不开硫酸。
| 沙场练兵 |  |
1. 为了防治酸雨,减少煤燃烧时向大气排放的SO2,工业上通过生石灰和含硫的煤混合使用可以“固硫”(避免硫化合物进入大气),最后生成石膏。试回答:
(1)整个“固硫”反应所涉及的反应类型包括:①化合②分解③置换④复分解⑤氧化还原反应⑥非氧化还原反应⑦离子反应⑧非离子反应(分子反应)。其中正确的是( )
A.①⑤⑥⑦ B.①②③⑤⑧ C.①⑤⑥⑧ D.②④⑤⑦
(2) 第一步“固硫”反应的化学方程式中所需气态物质的化学计量数之和为( )
A.1 B. 2 C.3 D.4
(3) 你认为减少酸雨产生可采取的措施是( )
①少用煤作燃料 ②把工厂的烟囱造高 ③先将燃料煤脱硫 ④在土壤中加石灰防止酸化 ⑤开发新能源,避免含S、N的氧化物大量排放
A.①②③ B.②③④⑤ C.①③⑤ D.①③④⑤
2.
有关接触法制硫酸的叙述正确的是
( )
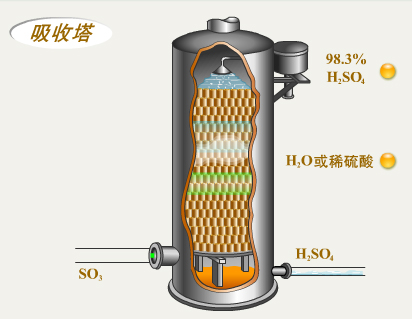
A. 吸收塔不得用水吸收三氧化硫
B. 进入接触室的SO2和空气混合物中的其它杂质必须除去
C. 硫酸厂的尾气要经碱液或氨水处理后才能排放
D. 用黄铁矿燃烧生成二氧化硫与用硫燃烧生产二氧化硫后者较复杂
3. 用硫铁矿制硫酸,若硫铁矿含杂质30%,杂质不与氧气反应,要得到98%的硫酸4t,工业上需要标准状况下空气多少立方米( )
A. 1680 B. 7340 C. 8400 D. 多于 8400
