| 发现之旅 |  |
在辽阔的化学领域中,绝大多数化学家都从事着实验发现的工作。这不仅仅因为实验是化学学科的传统,也由于化学研究对象的复杂性。当我们面对复杂体系的时候,在很多时候,通过实验来认识或深人理解几乎是惟一选择。在化学史上,有无数这样的实例来印证化学实验对于化学发展的重要性,例如Curie夫人发现镭的故事就是其中一个精彩的范例。
当我们强调化学实验的重要性时,也决不应当忽视理论对于化学探索的指导意义。的确,在化学发展的某些阶段,理论的突破会给化学带来突飞猛进的发展。一个突出的例子就是Linus Pauling关于化学键的理论:Pauling的价键理论不仅为人们认识化学键奠定了坚实的理论基础,它的影响也扩大到化学学科之外,对于相关领域的发展也起到了非常重要的作用。
| 深入思考 |  |
(1)无机物的性质:与原子结构有关。
(2)有机物的性质:与分子结构有关。
而有机物的分子结构又与官能团的种类和基团之间的相互影响有关.
二、性质实验方案设计的一般思路
分析结构→对比回顾相关知识→预测性质→拟定方案
分子结构 同系物 稳定性
原子结构 元素周期表 酸、碱性
氧化还原性
官能团反应
常识了解
三、性质实验方案的设计
1.证明酸性:(1)pH试纸或酸碱指示剂;(2)与
2.证明弱酸性:(1)证明存在电离平衡;(2)测定对应盐溶液酸碱性;(3)测定稀释前后pH的变化。
3.证明氧化性:与还原剂(如KI、
4.证明还原性:与氧化剂(如
5.证明为胶体分散系:有了达尔效应。
6.证明有碳碳双键(或三键):使溴水或酸性
7.证明酚羟基:(1)与浓溴水反应产生白色沉淀;(2)与
8.证明醛基:(1)与银氨溶液发生银镜反应;(2)与新制
9.证明醇羟基:与酸发生酯化反应,其产物不溶于水,有果香味.
10.比较金属的活动性:(1)与水反应;(2)与酸反应;(3)置换反应;(4)原电池;(5)电解放电顺序;(6)最高价氧化物对应水化物的碱性强弱;(7)对应盐的酸碱性强弱。
11.比较非金属的活动性:(1)置换反应;(2)与氢气反应快慢;(3)气态氢化物的稳定性、还原性;(4)最高价氧化物对应水化物的酸性强弱;(5)对应盐的酸碱性强弱;(6)与同种变价金属反应(如Cu、Fe),但注意例外。
12.比较酸(碱)的酸(碱)性强弱:较强的酸(碱)能制得较弱的酸(碱)。
| 学有所用 |  |
二氧化硫性质的组合实验
硫化氢的性质实验
| 沙场练兵 |  |
1. 有两个实验小组的同学为探究过氧化钠与二氧化硫的反应,都用如下图所示的装置进行实验。通入SO2气体,将带余烬的木条插入试管C中,木条复燃。
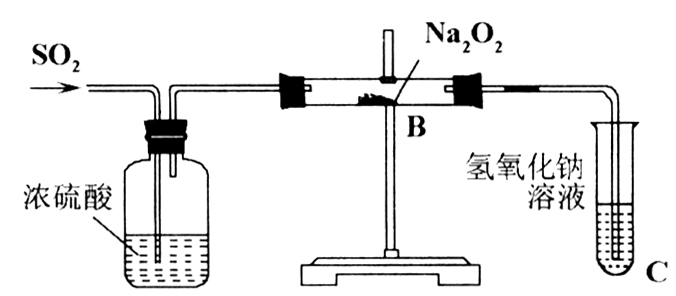
请回答下列问题:
(1)第1小组同学认为Na2O2与SO2反应生成了Na2SO3和O2,该反应的化学方程式是: 。
(2)请设计一种实验方案证明Na2O2与SO2反应生成的白色固体中含有Na2SO3 。
(3)第2小组同学认为Na2O2与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成。为检验是否有Na2SO4生成,他们设计了如下方案:

上述方案是否合理? 。
请简要说明两点理由:
① ;② 。

