| 发现之旅 |
 |
|
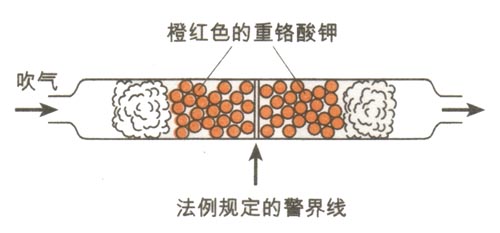
| 司机酒后驾车容易肇事,因此交通法规禁止酒后驾车。怎样判断驾车人是否为酒后驾车呢?一种科学的检测方法是使驾车人呼出的气体接触载有经过硫酸酸化处理的强氧化剂K2Cr2O7的硅胶。 |
|
K2Cr2O7是一种橙红色具有强氧化性的化合物,当它在酸条件下被还原成三价铬时,颜色变为绿色。据此,当交警发现汽车行驶不正常时,就可上前阻拦,并让司机对填充了吸附有K2Cr2O7的硅胶颗粒的装置吹气。若发现硅胶变色达到一定程度,即可证明司机是酒后驾车。这时酒精被氧化为醋酸:
|
2K2Cr2O7+3CH3CH2OH+8H2SO4→2K2SO4+2Cr2(SO4)3+3CH3COOH+11H2O |
|
测定酒精含量 |
| 深入思考 |
 |
|
| 我们知道,铁原子可以失去2个电子而显+2价,也可以失去3个电子而显+3价。那么如何来检验溶液中的离子是Fe2+还是Fe3+呢?我们来做这样一个实验: |
|
|
| 在实验中我们可以观察到,在没有加入氯水的时候,虽然也滴加了KSCN溶液,但是试管中的溶液颜色并没有发生变化。而加入氯水后溶液颜色变为血红色。 |
|
| 我们知道KSCN溶液能用来检验Fe3+,没有滴加氯水时溶液不变色,说明溶液中仍为Fe2+;当滴加氯水后,由于氯水中的氯气有强氧化性,将Fe2+氧化成Fe3+,Fe3+与KSCN溶液反应,而使溶液呈血红色。 |
2Fe2+ + Cl2 === 2Fe3++ 2Cl-
|
在这个反应式中,Fe2+转移电子给Cl2,使得Cl 化合价降低,而Fe 化合价升高。所以Fe2+是还原剂, Cl2 是氧化剂。
氧化剂是指在反应中得到电子的物质,也就是反应后所含元素化合价降低的物质。氧化剂具有氧化性,反应时本身被还原,生成物为还原产物。
还原剂是指在反应中失去电子的物质,也就是反应后所含元素化合价升高的物质。还原剂具有还原性,反应时本身被氧化,生成物为氧化产物。 |
|
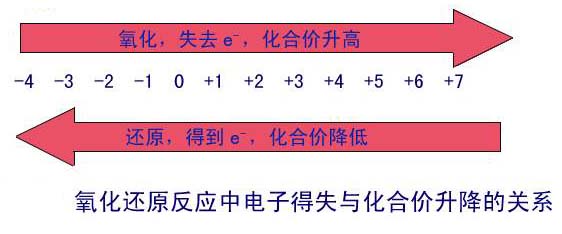
| 物质在反应中是作氧化剂还是作还原剂,主要决定于元素的化合价: |
当元素位于最高价时,它的原子只能得到电子,因此,该元素只能作为氧化剂。如: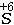 |
当元素位于最低价时,它的原子只能失去电子,因此,该元素只能作为还原剂。如: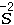 |
当元素位于中间价态时,它的原子既能得到电子,又能失去电子,因此,该元素既能作为氧化剂,又能作为还原剂。如: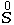 和 和 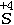 |
|
硫元素化合价的变化与氧化还原反应示意图 |
| 学有所用 |
 |
|
趣味实验 |
| 不用点火,就能用一支玻璃棒点燃酒精等灯。你相信吗? |
|
|
| 沙场练兵 |
 |
|
1. 需要加入氧化剂才能实现的变化是( )
A.MnO2→MnSO4
B.AlO2-→Al(OH)3
C.KI→KIO3
D.HNO3→NO
答案:C
解析:氧化剂在反应中是得到电子的物质,故题中正确的选项中物质的变化应是失去电子的变化。可以通过元素化合价是否升高来判断:A中的Mn由+4价降为+2价,D中的N由+5价降为+2价,MnO3、HNO3被还原,B中Al的价态反应前后无变化,无电子转移。C中的I由-1价升高为+5价,KI被氧化,作还原剂。
|
2. 在一定条件下,氯酸钾与碘按下式反应:2KClO3+I2=2KIO3+Cl2,由此可推断下列相应的结论,不正确的是( )
A. 该反应属于置换反应
B. 还原性I2>Cl2
C. 非金属性I>Cl
D.氧化性KClO3>Cl2
答案:C
解析:据置换反应的概念首先断定所给反应是一个置换反应。由元素化合价的变化可知:反应2KClO3+I2====2KIO3+Cl2中KClO3是氧化剂,I2是还原剂,KIO2是氧化产物,Cl2是还原产物,据“还原剂的还原性>还原产物的还原性”规律推知,B正确。再结合Cl2不能将I2氧化成IO3- 的事实,推知D正确,反应2KClO3+I2====2KIO3+Cl2的发生,与I元素、Cl元素的非金属性强弱没有必然联系,且事实上是Cl元素的非金属性强于I元素的非金属性,因而C是不正确的。
|
3.根据反应式①2Fe3++2I- ==== 2Fe2++I2 ②Br2+2Fe2+ ==== 2Br-+2Fe3+可判断离子还原性的强弱顺序为( )
A.Br-、Fe2+、I-
B.I-、Fe2+、Br-
C.Br-、I-、Fe2+
D.Fe2+、I-、Br-
答案:B
解析:首先确定各反应的还原剂(①为I-,②为Fe2+)和还原产物(①为Fe2+②为Br-),其次是根据还原剂的还原性强于还原产物的还原性,推出还原性:I->Fe2+,Fe2+>Br-,最后综合给出离子还原性强弱顺序为:I-、Fe2+、Br-。
|
4. 根据反应:①2A3++3B======2A+3B2+,②3D2++2A=====2A3++3D,③B2++C====C2++B,判断A、B、C、D的还原性由强到弱的顺序是( )
A. A>B>C>D
B. D>C>B>A
C. C>B>A>D
D. B>A>C>D
答案:C
解析:此题主要考查的是氧化―还原反应中的一条普通的规律,即氧化剂的氧化性大于氧化产物的氧化性,还原剂的还原性大于还原产物的还原性。在反应①中可知,还原性B>A。由反应②可知还原性A>D,由反应③可知还原性C>B。故由强到弱的顺序是C>B>A>D。
|
5. 下列说法中,正确的是( )
A.有新单质生成的化学反应,不一定是氧化还原反应
B.在氧化还原反应中,非金属单质都是氧化剂,金属单质都是还原剂
C.某元素从化合态变成游离态时,该元素一定被还原
D.金属阳离子被还原不一定得到金属单质
答案:A、C
解析:在白磷转变成红磷、石墨转化为金刚石的这些化学反应中,有新单质生成,但发生的不是氧化还原反应。“A”正确;
在反应 及反应 及反应 中,非金属单质都是做还原剂,故“B”不正确(因为金属元素无负价,“金属单质都是还原剂”此说法成立); 中,非金属单质都是做还原剂,故“B”不正确(因为金属元素无负价,“金属单质都是还原剂”此说法成立);
在反应 中,氯元素从化合态变到游离态,但不是被还原,而是化合价升高被氧化,“C”不正确; 中,氯元素从化合态变到游离态,但不是被还原,而是化合价升高被氧化,“C”不正确;
在反应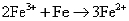 中,Fe3+ 被还原,产物不是单质而是Fe2+ ,“D”正确。 中,Fe3+ 被还原,产物不是单质而是Fe2+ ,“D”正确。 |
6. 根据下列反应的化学方程式:
①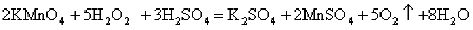
②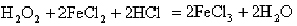
③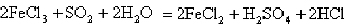
判断下列物质的氧化能力由大到小的顺序是( )
A.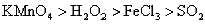
B.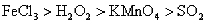
C.
D.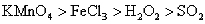
|
| |
|
| |
| |
| |









 及反应
及反应 中,非金属单质都是做还原剂,故“B”不正确(因为金属元素无负价,“金属单质都是还原剂”此说法成立);
中,非金属单质都是做还原剂,故“B”不正确(因为金属元素无负价,“金属单质都是还原剂”此说法成立); 中,氯元素从化合态变到游离态,但不是被还原,而是化合价升高被氧化,“C”不正确;
中,氯元素从化合态变到游离态,但不是被还原,而是化合价升高被氧化,“C”不正确;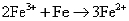 中,Fe3+ 被还原,产物不是单质而是Fe2+ ,“D”正确。
中,Fe3+ 被还原,产物不是单质而是Fe2+ ,“D”正确。 ;由②得,氧化性:
;由②得,氧化性: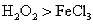 ;由③得:氧化性:
;由③得:氧化性: 。综合这三种情况,可知,氧化性:
。综合这三种情况,可知,氧化性: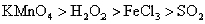 。故“
。故“