| 发现之旅 |  |


| 深入思考 |  |
例如:在餐具上镀铜。
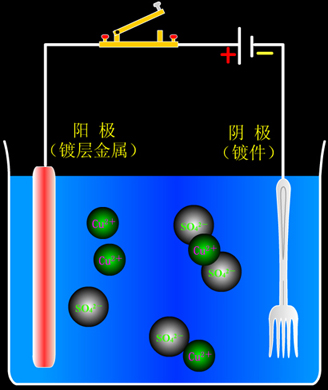
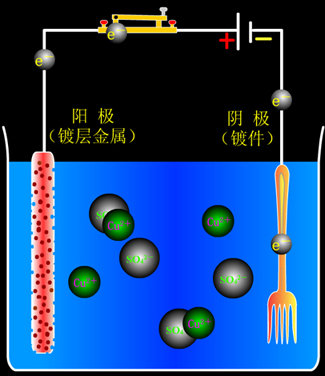
两个电极的反应式为:
阳极:Cu - 2e ==== Cu2+
阴极:Cu2+ + 2e ==== Cu
电镀是防止金属被腐蚀的一种重要方法,在金属制品表面镀上一层其他金属,如Zn、Sn、Cr和Ni等。这些金属能氧化而形成一层致密的氧化物薄膜,从而阻止水和空气等对金属制品的腐蚀。要注意的是,镀层金属要比待镀金属更活泼,也就是说:在发生腐蚀时是镀层金属被腐蚀,而待镀金属被保护起来了,并没有被腐蚀。
电镀工业的废水中含有剧毒物质,如:氰化物、重金属等。这些有毒物质随废水流入自然水域,会严重污染水体。所以这些废水在排放前必须经过处理,并挥手其中的有用成分,将有毒有害物质的浓度降低到符合工业废水排放标准。另外一种方法就是改变电镀液成分,采用无氰电镀工艺。
| 学有所用 |  |
电镀与环境保护
电镀生产过程中产生的废水、废气、废渣里含有多种对环境有害的物质,如果任意排放,会造成严重的环境污染。如电镀生产中产生的废水里往往含有酸、碱等废液,铬等重金属,还有苯类、硝基、胺类等有机物,有的还含有氰等;电镀废气中往往有酸碱废气、铬酸雾、氮氧化物、金属尘等。
电镀废水的治理方法有化学法、离子交换法、电解法、反渗透法、蒸发浓缩法和电渗析法等。
电镀废气的治理方法有加入一些表面活性剂抑制废气逸出和物理吸收法等。
废水、废气处理方法的选择应符合以下原则:
(1)处理质量要好,处理后应符合国家规定的排放标准,对其中的有用成分要回收利用。
(2)处理方法对废水变化的适应性要强,应能适应废水的浓度、pH、成分等变化。
(3)经济效益要好,所用处理设备的投资小,占地面积小。
(4)节约能源、资源,回收效益好。
| 沙场练兵 |  |
1. 在下列描述中,不符合生产实际的是( )
A. 电解熔融的氧化铝制取金属铝,用铁作阳极
B. 电解法精练粗铜,用纯铜作阴极
C. 电解饱和食盐水制烧碱,用涂镍碳钢作阴极
D. 在镀件上点镀锌,用锌作阳极
2. 下图中A为直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽。接通电路后发现B上的c点显红色。为实现铁上镀锌,接通K后,使c、d两点短路。下列叙述正确的是( )
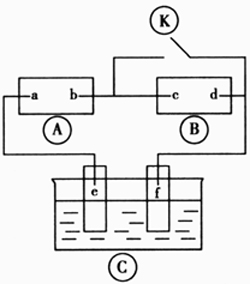
A. a 为直流电源的负极
B. c 极发生的反应为 2H+ + 2e- === H2↑
C. f 电极为锌板
D. e 极发生还原反应
3. 下列有关电化学的图示中,完全正确的是( )

4. 下列关于图15-19的说法,正确的是( )
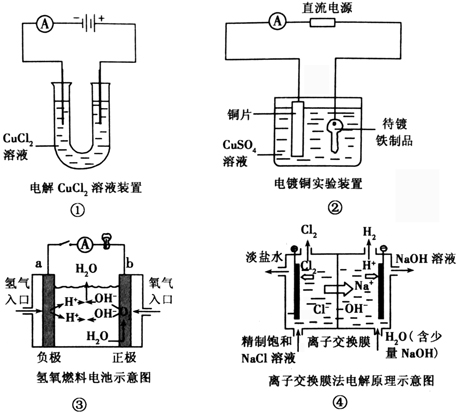
A. ①装置中阴极处产生的气体能够使湿润淀粉KI试纸变蓝
B. ②装置中待镀铁制品应与电源正极相连
C. ③装置中电子由b极流向a极
D. ④装置中的离子交换膜可以避免生成的Cl2与NaOH溶液反应
5. 有下列四个装置
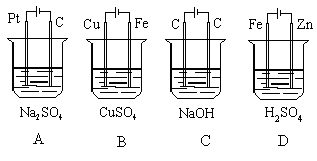
(1)其中能用于电镀的是( )
(2)电解一段时间后,其阴极与阳极附近溶液pH值都无明显变化的是( )
(3)电解一段时间,溶液pH值增大的是( )
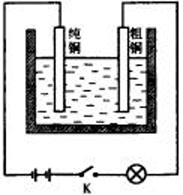
6. 如下图所示,在水泥槽里放入蒸馏水,在蒸馏水中放入一块纯铜板和一块粗铜板作电极,用导线连接电源、开关和一个阻值4欧的灯泡。合上开关K,小灯泡将 ,然后断开开关,再加入适量无水硫酸铜,待全部溶解后,溶液将呈 色。这时若合上开关K,小灯泡将 ,纯铜板上发生的现象是 ,其电极反应式为 ;粗铜板上发生的现象是 。若测得此过程中1秒内共有3×10个18Cu2+和2×1018个SO42-通过两极板间某一截面,则加在灯泡两端的电压为 。
 上的c点显红色可判断出,c点由于H+放电生成OH-,即c为阴极、所以b为直流电源的负极。
上的c点显红色可判断出,c点由于H+放电生成OH-,即c为阴极、所以b为直流电源的负极。