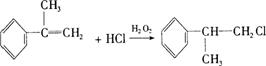
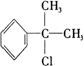
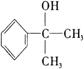
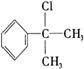
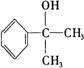
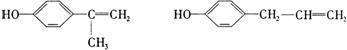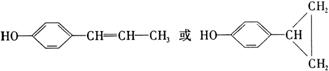–і‘Џ«∞√жµƒї∞ Ќђ—І√«£ђƒг√«Ї√£° їґ”≠ƒгЇЌќ“√«“ї∆рљш»лЄя»эїѓ—І„®ћвЄіѕ∞£° ќ“√«љЂ‘ЏљсЇуµƒ16÷№ ±Љдјпґ‘Ћщ—Ієэµƒїѓ—І÷™ ґ∞іїѓ—Іїщ±ЊЄ≈ƒо°Ґїѓ—Іїщ±Њјн¬џ°Ґ‘™ЋЎїѓЇѕќп°Ґ”–їъїѓЇѕќп°Ґїѓ—І µ—й°Ґїѓ—ІЉ∆Ћгµ»ƒЏ»ЁЈ÷њйЄіѕ∞°£Ќђ ±£ђќ“√«їєїбЄщЊЁЄіѕ∞µƒљшґ»£ђЉ∞ ±ћбє©“ї–©”≈–гµƒЄяњЉƒ£ƒв ‘ћв£ђє©„‘ќ“Љм≤в ± є”√°£ ±Њ∆Џќ“√«ћбє©ЅЋ“ї–©їщі°µƒЉм≤в ‘ћв£ђ«лƒг≤їљи÷ъ»ќЇќ≤ќњЉ й£ђ»ѕ’ж„чір£ђњіњіƒгƒ№µ√ґа…ўЈ÷£ђ“‘±г”ЏљсЇу”–µƒЈ≈ ЄµЎљш––Єіѕ∞°£ Ќђ—І√«£ђЄя»эƒкЉґµƒ—Іѕ∞…ъїо≥д¬ъљф’≈£ђ“≤±•Їђ∆Џіэ°£ѕ÷‘Џ’эµ±њ™—І£ђƒг”–√ї”–„цЇ√„Љ±Є£ђ ’ ∞––ƒ“£ђ»ЂЅ¶“‘Є∞ќ™ µѕ÷„‘ЉЇµƒ»Ћ…ъ√ќѕлґшЈ№ґЈƒЎ£њ і”љсћмњ™ Љ£ђќ“√«љЂЇЌƒгЌђ––£° Єя»эїѓ—Іњ™—ІЉм≤в ѕаґ‘‘≠„”÷ Ѕњ£ЇH µЏҐсЊн£®—°‘сћв£ђє≤70Ј÷£© “ї°Ґ—°‘сћв£®±Њћв∞ьј®10–°ћв£ђ√њ–°ћв3Ј÷£ђє≤30Ј÷£ђ√њ–°ћв÷ї”–“їЄц—°ѕоЈыЇѕћв“в£© 1£Ѓѕ¬Ѕ–Єч„йќп÷ µƒЊІће£ђїѓ—ІЉьја–ЌѕаЌђ£ђЊІћеја–Ќ“≤ѕаЌђµƒ « A£Ѓ
2£Ѓ„ољьњ∆—ІЉ“ЈҐѕ÷ЅЋ—х‘™ЋЎµƒ“ї÷÷–¬µƒЅ£„”
A£ЃЋь «—х‘™ЋЎµƒ“ї÷÷ЌђЋЎ“м–ќће B£ЃЋь «—х‘™ЋЎµƒ“ї÷÷ЌђќїЋЎ C£ЃЋьµƒƒ¶ґы÷ Ѕњќ™
3£Ѓѕ¬Ѕ–ќп÷ Љ”»лЋЃ÷–£ђƒ№ єЋЃµƒµзјл≥ћґ»‘ціу£ђ«“Ћщµ√»№“Їѕ‘Ћб–‘µƒ « A£Ѓ
4£Ѓѕ¬Ѕ–ѕ÷ѕуїт”¶”√÷–£ђ≤ї…жЉ∞љЇће–‘÷ µƒ « A£Ѓ‘Џ±•ЇЌ¬»їѓћъ»№“Ї÷–÷рµќЉ”»лNaOH»№“Ї£ђ≤ъ…ъЇмЇ÷…Ђ≥Ѕµн B£Ѓ«е≥њ£ђ‘Џ√ѓ√№µƒ чЅ÷÷–£ђ≥£≥£њ…“‘њіµљі”÷¶“ґЉдЌЄєэµƒµјµјєв÷щ C£Ѓ”√∞лЌЄƒ§Ј÷јлµнЈџЇЌ ≥—ќµƒїмЇѕ“Ї D£Ѓ…цє¶ƒ№Ћ•љяµ»Љ≤≤°“э∆рµƒ—™“Ї÷–ґЊ£ђњ…јы”√—™“ЇЌЄќцљш––÷ќЅ∆ 5£Ѓ«в∆ш «»Ћја„ојнѕлµƒƒ№‘і°£“—÷™‘Џ A£Ѓ
B£Ѓ
C£Ѓ
D£Ѓ
6£Ѓѕ¬Ѕ–єЎ”ЏЌ≠µзЉЂµƒ–р ц÷–’э»Јµƒ « A£ЃЌ≠–њ‘≠µз≥Ў÷–Ќ≠ «ЄЇЉЂ B£Ѓ”√µзљвЈ®ЊЂЅґі÷Ќ≠ ±і÷Ќ≠„ч—фЉЂ C£Ѓ‘Џћъ…ѕµзґ∆“ш ±”√Ќ≠„ч“хЉЂ D£Ѓµзљвѕ°ЅтЋб ±”√Ќ≠„ч—фЉЂ£ђ—фЉЂ≤ъќпќ™—х∆ш 7£Ѓƒњ«∞£ђњ∆—ІЉ“ƒвЇѕ≥…“ї÷÷°∞ґю÷Ўєє‘м°±µƒ«т–ќЈ÷„”£ђЉі∞—„г«т–Ќµƒ
A£ЃЋь «”…Ѕљ÷÷µ•÷ „й≥…µƒїмЇѕќп B£ЃЋь «“ї÷÷єиЋб—ќ C£ЃЋь «“ї÷÷–¬–ЌїѓЇѕќп D£ЃЋь «“ї÷÷ЄяЊџќп 8£Ѓ“їґ®ћхЉюѕ¬£ђ∞±∆ш”л“ї—хїѓµ™ЈҐ…ъЈі”¶£Ї
A£Ѓ2 £Ї3 B£Ѓ3 £Ї 9£Ѓѕ¬Ѕ–”–їъќп÷–£ђЉ»ƒ№ЈҐ…ъЉ”≥…Јі”¶£ђ”÷ƒ№ЈҐ…ъх•їѓЈі”¶£ђїєƒ№±ї–¬÷∆±Єµƒ
A£Ѓ
C£Ѓ
10£Ѓѕ¬Ѕ–≥э»•‘”÷ Ћщ”√ ‘ЉЅїтЈљЈ®інќуµƒ « A£Ѓ≥э»•
B£Ѓ≥э»•±љ÷–»№”–µƒ…ўЅњ±љЈ”£ЇЉ”»л ЅњNaOH»№“Ї£ђЈі”¶ЇуЈ÷“Ї C£Ѓ≥э»•““Ћб““х•÷–їм”–µƒ…ўЅњ““Ћб£ЇЉ”»л““іЉ≤ҐЉ”»» D£Ѓ≥э»•
ґю°Ґ—°‘сћв£®±Њћв∞ьј®10–°ћв£ђ√њ–°ћв4Ј÷£ђє≤40Ј÷£ђ√њ–°ћв÷ї”–“їЄц—°ѕоЈыЇѕћв“в£© 11£Ѓ
A£Ѓ≥£ќ¬≥£—єѕ¬£ђ B£Ѓ C£Ѓ58.5gNaClЊІће÷–ЋщЇђµƒ¬»їѓƒ∆Ј÷„” эƒњќ™
D£Ѓ
12£Ѓt°ж ±£ђЉ„°Ґ““ЅљЄц…’±≠÷–Єч Ґ”–≈®ґ»ѕаЌђ°Ґ÷ Ѕњѕаµ»µƒ≤ї±•ЇЌµƒKCl»№“Ї£ђ“їЈЁ’фЈҐµфm gЋЃ£ђјд»іµљ‘≠ќ¬ґ»£ђќц≥цa gЊІће£®≤їЇђљбЊІЋЃ£©£їЅн“їЈЁ’фЈҐµфn gЋЃ£ђјд»іµљ‘≠ќ¬ґ»£ђ≤р≥цb gЊІће°£‘тt°ж ±KClµƒ»№љвґ» « A£Ѓ
13£ЃљЂ
A£Ѓ
C£Ѓ
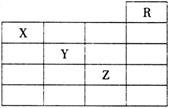
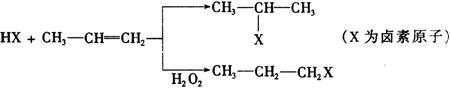
14£Ѓ»зЌЉ «‘™ЋЎ÷№∆Џ±нµƒ“ї≤њЈ÷£ђєЎ”Џ‘™ЋЎX°ҐY°ҐZµƒ–р ц’э»Јµƒ «
ҐўXµƒ∆шћђ«вїѓќп”лYµƒ„оЄяЉџ—хїѓќпґ‘”¶µƒЋЃїѓќпƒ№ЈҐ…ъЈі”¶…ъ≥…—ќ ҐЏY°ҐZµƒ∆шћђ«вїѓќпЋЃ»№“ЇµƒЋб–‘Y£ЉZ ҐџZµƒµ•÷ ‘Џ≥£ќ¬ѕ¬ «“Їће£ђњ…”лћъЈџЈі”¶ Ґ№Zµƒ‘≠„”–т э±»Yіу19 ҐЁZЋщ‘Џµƒ÷№∆Џ÷–Їђ”–32÷÷‘™ЋЎ A£ЃҐўҐЏҐџҐ№ B£ЃҐўҐЏҐџҐ№ҐЁ C£Ѓ÷ї”–Ґџ D£Ѓ÷ї”–ҐўҐ№ 15£ЃЄщЊЁµ»µз„”‘≠јн£ђ”…ґћ÷№∆Џ‘™ЋЎ„й≥…µƒЅ£„”£ђ÷ї“™∆д‘≠„” эѕаЌђ£ђЄч‘≠„”µƒ„оЌв≤гµз„” э÷ЃЇЌ“≤ѕаЌђ£ђњ…ї•≥∆ќ™µ»µз„”ће°£µ»µз„”ће÷ЃЉдљбєєѕаЋ∆°Ґќпјн–‘÷ ѕаљь°£“‘ѕ¬Єч„йЅ£„”≤їƒ№ї•≥∆ќ™µ»µз„”ћеµƒ « A£Ѓ
16£Ѓѕ¬Ѕ–јл„”Јљ≥ћ љ÷– й–і’э»Јµƒ « A£ЃЅтЋб—«ћъ»№“Ї÷–Љ”»л”√ЅтЋбЋбїѓµƒєэ—хїѓ«в»№“Ї£Ї
B£Ѓћъ”лѕ°ЅтЋбЈі”¶£Ї
C£Ѓѕт¬»їѓ¬Ѕ»№“Ї÷–Љ”»лєэЅњµƒ∞±ЋЃ£Ї
D£ЃћЉЋб«в∞і»№“Ї÷–Љ”»лєэЅњµƒ«в—хїѓƒ∆»№“Ї£Ї
17£ЃљЂ“їґ®ЅњFeЇЌ
A£Ѓ45mL B£Ѓ50mL C£Ѓ40mL D£ЃќёЈ®»Јґ® 18£ЃѕгјЉЋЎµƒљбєєЉт љ»зѕ¬ЌЉЋщ Њ£ђЋь”–“Ћ»Ћµƒ∆шќґ£ђіж‘Џ”Џѕг≤Ёґє°Ґѕг÷ђ°Ґ∞≤ѕҐѕг°Ґґ°„””ЌЇЌѕг√©”Ќ÷–£ђ «÷∆„ч«…њЋЅ¶µƒЄ®÷ъ‘≠Ѕѕ°£ѕ¬Ѕ–єЎ”ЏѕгјЉЋЎµƒ≈–ґѕ≤ї’э»Јµƒ «
A£Ѓњ…”л“ш∞±»№“ЇЈі”¶ B£Ѓњ…”л«в—хїѓƒ∆»№“ЇЈі”¶ C£ЃЈ÷„”÷–Ћщ”–‘≠„”ґЉ‘ЏЌђ“ї∆љ√ж…ѕ D£Ѓњ…”л≈®деЋЃЈҐ…ъ»°іъЈі”¶ 19£Ѓ”√»№÷ µƒќп÷ µƒЅњ≈®ґ»Њщќ™
A£Ѓ
20£Ѓ”–“ї∆њќё…Ђ»№“Ї£ђњ…ƒ№Їђ”–
A£Ѓњѕґ®”–
C£Ѓњѕґ®”–
µЏҐтЊн£®Ј«—°‘сћв£ђє≤80Ј÷£© „Ґ“в ¬ѕо£Ї 1£Ѓ”√Є÷± їт‘≤÷й± љЂір∞Є÷±љ”–і‘Џ ‘Њн÷–°£ 2£ЃірЊн«∞љЂ√№ЈвѕяƒЏµƒѕоƒњћо–і«е≥ю°£»фћо‘ЏѕяЌв£ђ ‘Њн„чЈѕ°£ 3£Ѓ±ЊЊнє≤7–°ћв£ђє≤80Ј÷°£ »э°Ґ£®±Њћв∞ьј®2–°ћв£ђє≤20Ј÷£© 21£Ѓ£®8Ј÷£©љЂ
£®1£©іп∆љЇв ±£ђ
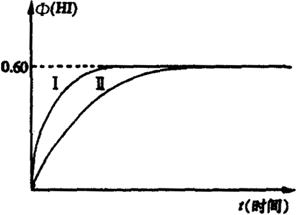
£®2£©»фЄƒ±дЈі”¶ћхЉю£ђ‘Џƒ≥ћхЉюѕ¬
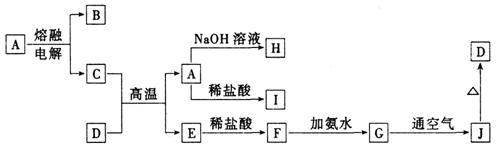
ҐўЇг»ЁћхЉюѕ¬£ђ…эЄяќ¬ґ» ҐЏЇг»ЁћхЉюѕ¬£ђљµµЌќ¬ґ» ҐџЇгќ¬ћхЉюѕ¬£ђЋх–°Јі”¶»Ё∆чћеїэ Ґ№Їгќ¬ћхЉюѕ¬£ђј©іуЈі”¶»Ё∆чћеїэ ҐЁЇгќ¬°ҐЇг»ЁћхЉюѕ¬£ђЉ”»л µ±іяїѓЉЅ £®3£©»ф±£≥÷ќ¬ґ»≤ї±д£ђ‘ЏЅн“їѕаЌђµƒ 22£Ѓ£®12Ј÷£©”–A°ҐB°ҐC°ҐD°ҐEќе÷÷ґћ÷№∆Џ‘™ЋЎ£ђЋь√«µƒ‘≠„”–т э“јіќ‘ціу°£“—÷™£ЇAЇЌC°ҐBЇЌDЈ÷±рќї”ЏЌђ÷ч„е£ђ«“B°ҐD÷ „” э÷ЃЇЌ «A°ҐC÷ „” э÷ЃЇЌµƒ2±ґ£їE‘ЏЌђ÷№∆Џ‘™ЋЎ÷–‘≠„”∞лЊґ„о–°°£ £®1£©
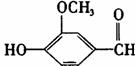
£®2£©”…A°ҐB°ҐC°ҐDЋƒ÷÷‘™ЋЎ–ќ≥…µƒЅљ÷÷їѓЇѕќпѕаї•ЉдЈі”¶µƒјл„”Јљ≥ћ љќ™____________________________°£ £®3£©A°ҐB°ҐC»э÷÷‘™ЋЎЋщ–ќ≥…µƒїѓЇѕќпµƒµз„” љќ™________°£ £®4£©”√ґањ„µƒ ѓƒЂµзЉЂµзљвµќ”–Ј”ћ™µƒCЇЌE–ќ≥…µƒїѓЇѕќпµƒ±•ЇЌ»№“Ї°£љ”Ќ®µз‘і“їґќ ±ЉдЇу£ђ________ЉЂ£®ћоµзЉЂ√ы≥∆£©Єљљь≥цѕ÷Їм…Ђ£їЅн“їЉЂµƒµзЉЂЈі”¶ љќ™________________£ђњ…”√________Љм—йЄ√ЉЂЋщµ√≤ъќп°£ Ћƒ°Ґ£®±Њћв∞ьј®2–°ћв£ђє≤22Ј÷£© 23£Ѓ£®10Ј÷£©A°™J «÷–—Іїѓ—І≥£Љыµƒќп÷ £ђЋь√«÷ЃЉдµƒ„™їѓєЎѕµ»зѕ¬ЌЉЋщ Њ£®≤њЈ÷≤ъќп“—¬‘»•£©°£“—÷™A «“ї÷÷Єя»џµгќп÷ £ђD «“ї÷÷Їм„Ў…Ђєћће£ђHµƒ—ж…ЂЈі”¶≥ ї∆…Ђ°£
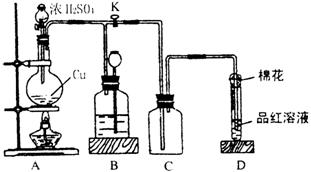
«лїЎірЅЋЅ–ќ ћв£Ї £®1£©Aќп÷ µƒїѓ—І љќ™________£ђHќп÷ µƒ√ы≥∆ќ™________________°£ £®2£©G°ъJµƒїѓ—ІЈљ≥ћ љќ™________________°£ £®3£©Dќп÷ ”л—ќЋб«°Ї√Јі”¶µƒјл„”Јљ≥ћ љќ™________________£ђЋщµ√»№“Їѕ‘Ћб–‘µƒ‘≠“т «________________£®”√јл„”Јљ≥ћ љ±н Њ£©°£ 24£Ѓ£®12Ј÷£©ƒ≥їѓ—І–Ћ»§–°„йќ™ћљЊњЌ≠Єъ≈®ЅтЋбµƒЈі”¶£ђ”√ѕ¬ЌЉЋщ Њ„∞÷√љш––”–єЎ µ—й°£«лїЎір£Ї
£®1£©„∞÷√A÷–ЈҐ…ъµƒїѓ—ІЈі”¶Јљ≥ћ љќ™________________________°£ £®2£©„∞÷√D÷– ‘є№њЏЈ≈÷√µƒ√ёї®÷–”¶љю“ї÷÷“Їће£ђ’в÷÷“Їће «___________________£ђ∆д„ч”√ «________________________________________°£ £®3£©„∞÷√Bµƒ„ч”√ «÷ьіжґа”аµƒ∆шће°£µ±Dі¶”–√чѕ‘µƒѕ÷ѕуЇу£ђєЎ±’–э»ыK£ђ“∆»•Њ∆ЊЂµ∆£ђµЂ”…«І”а»»µƒ„ч”√£ђAі¶»‘”–∆шће≤ъ…ъ£ђіЋ ±B÷–ѕ÷ѕу «_______________________°£B÷–”¶Ј≈÷√µƒ“Їће «£®ћо„÷ƒЄ£©________________°£ a£ЃЋЃ b£ЃЋб–‘
£®4£© µ—й÷–£ђ»°“їґ®÷ ЅњµƒЌ≠∆ђЇЌ“їґ®ћеїэ
Ґў”–“їґ®Ѕњµƒ”аЋбµЂќіƒ№ єЌ≠∆ђЌк»Ђ»№љв£ђƒг»ѕќ™‘≠“т «_____________________°£ ҐЏѕ¬Ѕ–“©∆Ј÷–ƒ№”√јі÷§√чЈі”¶љб шЇуµƒ…’∆њ÷–»Ј”–”аЋбµƒ «________________£®ћо„÷ƒЄ£©°£ a£ЃћъЈџ b£Ѓ
ќе°Ґ£®±Њћв∞ьј®2–°ћв£ђє≤24Ј÷£© 25£Ѓ£®8Ј÷£©“—÷™ƒ≥”–їъќпµƒљбєєЉт љќ™£Ї
£®1£©Є√”–їъќп÷–ЋщЇђєўƒ№Ќ≈µƒ√ы≥∆ «_______________________________________°£ £®2£©Є√”–їъќпЈҐ…ъЉ”≥…ЊџЇѕЈі”¶Їу£ђЋщµ√≤ъќпµƒљбєєЉт љќ™_____________________°£ £®3£©–і≥цЄ√”–їъќпЈҐ…ъѕы»•Јі”¶µƒїѓ—ІЈљ≥ћ љ£®„Ґ√чЈі”¶ћхЉю£©£Ї ____________________________________________________________________ 26£Ѓ£®16Ј÷£©”–їъїѓ—ІЈі”¶“тЈі”¶ћхЉю≤їЌђ£ђњ……ъ≥…≤їЌђµƒ”–їъ≤ъ∆Ј°£јэ»з£Ї £®1£©
£®2£©±љµƒЌђѕµќп”묱ЋЎµ•÷ їмЇѕ£ђ»ф‘Џєв’’ћхЉюѕ¬£ђ≤аЅі…ѕµƒ«в‘≠„”±ї¬±ЋЎ‘≠„”»°іъ£ї»ф‘ЏіяїѓЉЅ„ч”√ѕ¬£ђ±љїЈ…ѕµƒ«в‘≠„”±ї¬±ЋЎ‘≠„”»°іъ°£ є§“µ…ѕјы”√…ѕ ц–≈ѕҐ£ђ∞іѕ¬Ѕ–¬ЈѕяЇѕ≥…љбєєЉт љќ™
«лЄщЊЁ…ѕ ц¬Јѕя£ђїЎірЅЋЅ–ќ ћв£Ї £®1£©AµƒљбєєЉт љњ…ƒ№ќ™________________________°£ £®2£©Јі”¶Ґў°ҐҐџ°ҐҐЁµƒЈі”¶ја–ЌЈ÷±рќ™_________°Ґ_________°Ґ_________°£ £®3£©Јі”¶Ґ№µƒїѓ—ІЈљ≥ћ љќ™£®”–їъќп–іљбєєЉт љ£ђ≤Ґ„Ґ√чЈі”¶ћхЉю£©£Ї __________________________________________________________°£ £®4£©є§“µ…ъ≤ъ÷–£ђ÷–Љд≤ъќпA–лЊ≠Јі”¶ҐџҐ№ҐЁµ√D£ђґш≤ї≤…»°÷±љ”„™їѓќ™DµƒЈљЈ®£ђ∆д‘≠“т «_____________________________________________°£ £®5£©’в÷÷ѕгЅѕЊя”–ґа÷÷ЌђЈ÷“мєєће£ђ∆д÷–ƒ≥–©ќп÷ ”–ѕ¬Ѕ–ћЎ’ч£ЇҐў∆дЋЃ»№“Ї”ц
Ѕщ°Ґ£®±Њћв∞ьј®1–°ћв£ђє≤14Ј÷£© 27£Ѓ£®14Ј÷£©ѕ÷”–µ»ќп÷ µƒЅњµƒ
£®1£©Є√їмЇѕќп÷–
£®2£©»зєыЈі”¶Їу—ќЋб≤ї„гЅњ£ђ“™Љ∆Ћг…ъ≥…
£®3£©»фЄ√їмЇѕќп”л—ќЋб«°Ї√Ќк»ЂЈі”¶£ђ‘т—ќЋб÷–HClµƒќп÷ µƒЅњ≈®ґ»ќ™ґа…ў£њ£®«л–і≥цЉ∆Ћгєэ≥ћ£© £®4£©»ф
≤ќњЉір∞ЄЉ∞∆јЈ÷±к„Љ µЏҐсЊн£®1°™10ћв√њ–°ћв3Ј÷£ђ11°™20ћв√њ–°ћв4Ј÷£ђє≤70Ј÷£© 1£ЃD 2£ЃB 3£ЃB 4£ЃA 5£ЃC 6£ЃB 7£ЃC 8£ЃA 9£ЃD 10£ЃC 11£ЃB 12£ЃA 13£ЃB 14£ЃA 15£ЃD 16£ЃC 17£ЃC 18£ЃC 19£ЃB 20£ЃD µЏҐтЊн£®є≤80Ј÷£© 21£Ѓ£®є≤ 8Ј÷£©£®l£©£®2Ј÷£©0.05£ї £®2£©£®2Ј÷£©ҐџҐЁ£ї £®3£©£®4Ј÷£©2b£≠ 22£Ѓ£®є≤12Ј÷£©£®l£©£®lЈ÷£©
£®2£©£®2Ј÷£©
£®4£©£®1Ј÷£©“х£ї£®2Ј÷£©
23£Ѓ£®є≤10Ј÷£ђ√њњ’2Ј÷£©£®l£©
£®2£©
£®3£©
24£Ѓ£®є≤12Ј÷£©£®1£©£®2Ј÷£©
£®2£©£®√њњ’1Ј÷£©Љо“Ї£®∆дЋыЇѕјнір∞ЄЊщњ…ЄшЈ÷£©£їќь ’ґа”аµƒґю—хїѓЅт£ђЈј÷єќџ»Њњ’∆ш £®3£©£®√њњ’2Ј÷£© ‘ЉЅ∆њ÷–“Ї√жѕ¬љµ£ђ≥§Њ±¬©ґЈ÷–“Ї√ж…ѕ…э£їd £®4£©£®√њњ’2Ј÷£©ҐўЈі”¶єэ≥ћ÷–≈®ЅтЋб±їѕыЇƒ£ђ÷рљ•±дѕ°£ђґшЌ≠≤їЇЌѕ°ЅтЋбЈі”¶ ҐЏa°Ґd 25£Ѓ£®є≤8Ј÷£©£®1£©£®Єч2Ј÷£©ћЉћЉЋЂЉь°Ґф«їщ£ї £®2£©£®2Ј÷£©
£®3£©£®2Ј÷£©
26£Ѓ£®є≤16Ј÷£© £®1£©£®Єч1Ј÷£©
£®2£©£®Єч2Ј÷£©Љ”≥…£їѕы»•£їЋЃљвїт»°іъ £®3£©£®2Ј÷£©
£®4£©£®2Ј÷£©
£®5£©£®Єч2Ј÷£©
£®їт
27£Ѓ£®є≤14Ј÷£©£®1£©£®2Ј÷£©84 £Ї100 £®2£©£®√њњ’2Ј÷£©—ќЋб÷–HClќп÷ µƒЅњ≈®ґ»£ї»зєы—ќЋб£ђ≤ї„гЅњ£ђ”¶Є√“‘HClµƒќп÷ µƒЅњќ™Љ∆Ћг±к„Љ£ђ‘т±Ў–л÷™µј—ќЋб÷–HClµƒќп÷ µƒЅњ≈®ґ»°£ £®3£©£®4Ј÷£©
£®4£©£®4Ј÷£©
|