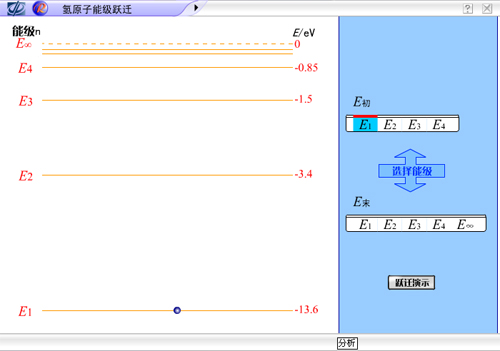
一、玻尔的原子模型
1.原子的稳定性.
经典的电磁理论认为电子绕原子核旋转,由于电子辐射能量,因此随着它的能量减少,电子运行的轨道半径也减小,最终要落入原子核中.
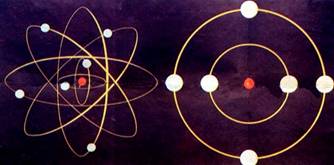
玻尔在1913年结合普朗克的量子理论针对这一问题提出新的观点.
玻尔假设一:原子只能处于一系列不连续的能量状态中,在这些状态中原子是稳定的,电子虽然绕核运动,但并不向外辐射能量.
说明:这一说法和事实是符合得很好的,电子并没有被库仑力吸引到核上,就像行星绕着太阳运动一样.这里所说的稳定的能量状态是指原子可能的一种能量状态,有某一数值的能量,这些能量包含了电子的动能和电势能的总和.
2.原子发光的光谱
经典的电磁理论认为电子绕核运行的轨道不断的变化,它向外辐射电磁波的频率应该等于绕核旋转的频率.因此原子辐射一切频率的电磁波,大量原子的发光光谱应该是连续光谱.
玻尔针对这一问题提出新的观点.
玻尔假设二:原子从一种稳定状态( ![]() )跃迁到另一种稳定状态(
)跃迁到另一种稳定状态( ![]() )时,它辐射(或吸收)一定频率的光子,光子的能量由这两种状态的能量差决定,即:
)时,它辐射(或吸收)一定频率的光子,光子的能量由这两种状态的能量差决定,即: ![]() .
.
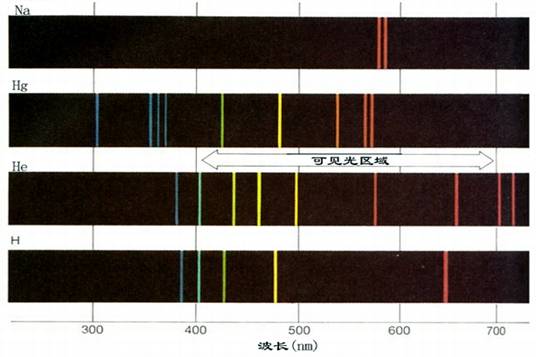
分光谱线
3.原子能量状态和电子轨道
玻尔假设三:原子的不同能量状态跟电子沿不同的圆形轨道绕核运动相对应.这些稳定的能量状态是不连续的,因此电子的可能轨道的分布也是不连续的.
二、氢原子的轨道半径和能量
玻尔从上述假设出发,利用库仑定律和牛顿运动定律,计算出了氢的电子可能的轨道半径和对应的能量.
根据计算结果概括为公式:
![]() ,
, ![]() ,
, ![]()
说明:公式中![]() 、
、 ![]() 和
和![]() 、
、![]() 的意义,并说明
的意义,并说明 ![]() 是正整数,叫做量子数,
是正整数,叫做量子数,
![]() m,
m, ![]() eV.
eV.
![]() 时,相应的能量为:
时,相应的能量为:
![]() eV、
eV、![]() eV、
eV、![]() eV…
eV…
![]()
三、氢原子的能级
氢原子的各种稳定状态时的能量值叫做能极,根据以上的计算,可画出示意的能级图. 原子最低能级所对应的能量稳定状态叫做基态,比基态能量高的能量稳定状态叫激发态.
原子从基态向激发态跃迁,电子克服库仑引力做功增大电势能,原子的能量增加要吸收能量.
原子也可以从激发态向基态跃迁,电子所受库仑力做正功减小电势能,原子的能量减少要辐射出能量,这一能量以光子的形式放出.
明确:原子的能量增加是因为电子增加的电势能大于电子减少的动能;反之原子的能量减少是因为电子减少的电势能大于电子增加的动能.
原子无论吸收能量还是辐射能量,这个能量不是任意的,而是等于原子发生跃迁的两个能级间的能量差.
明确:一个原子可以有许多不同的能量状态和相应的能级,但在某一时刻,一个原子不可能既处于这一状态也处于那一状态.如果有大量的原子,它们之中有的处于这一状态,有的处于那一状态.氢光谱的观测就说明了这一事实,它的光谱线不是一个氢原子发出的,而是不同的氢原子从不同的能级跃迁到另一些不同能级的结果.
氢原子的光谱线

分析越王勾践宝剑成分 漆碗(光谱分析进行考古研究)