| 发现之旅 |  |
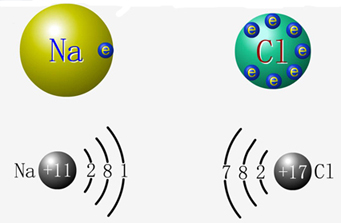
氯化钠的形成
| 深入思考 |  |
元素的“化合价”是元素的一种重要性质,这种性质只有跟其他元素相化合时才表现出来。就是说,当元素以游离态存在时,即没有跟其他元素相互结合成化合物时,该元素是不表现其化合价的,因此单质中元素的化合价为“0”。例如Zn、C、H2等。
那么化合价应该怎么来表示呢?一般我们把化合价的正、负与数值标在元素符号的正上方。如: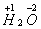 。
。
说明:离子的表示:元素符号的右上角先写电荷数,再写电量如:Na+, Mg2+, Cl-, SO42-。
元素化合价的表示:在元素符号的正上方先表示正、负号,再标明化合价数值。
如: 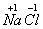 、
、 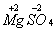 、
、 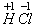 、
、 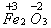
 |
 |
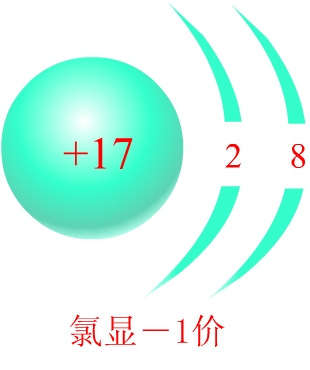 |
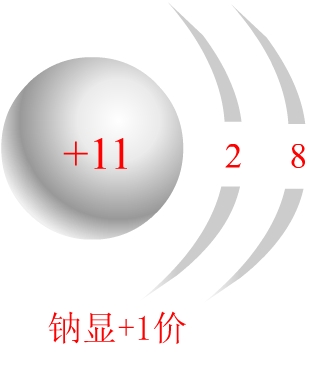
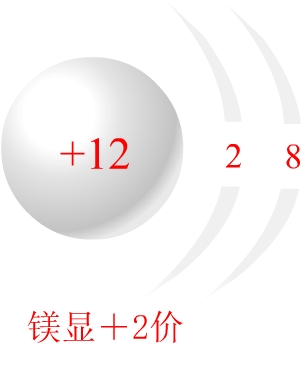
在化合物里,金属元素显正价,非金属元素通常显负价,非金属跟氧化合时则显正价。氢在化合物中通常显+1价,氧通常显-2价。这是为什么呢?
1.金属元素原子的最外层电子数比较少,在化学反应中易失电子,故显正价;非金属元素的原子最外层电子数比较多,在化学反应中易得电子而显负价。但在非金属氧化物里,由于氧原子吸引电子的能力比其他非金属原子强,共用电子对偏离非金属原子,偏向氧原子,所以非金属显正价,氧显负价。
3.在所有的非金属元素中,氧夺取电子的能力仅次于氟。氧最外层有6个电子,当氧与金属化合时,很容易得2个电子形成氧阴离子而显-2价。与其他非金属化合时,共用电子对偏向氧原子显-2价。
5.不同元素相化合时,一般都要使原子的最外层形成8个电子的稳定结构,所以最高正价与负价的绝对值之和等于8。
可见,元素的化合价主要是由最外层电子数决定的(有的跟次外层电子甚至倒数第三层电子也有关系)。
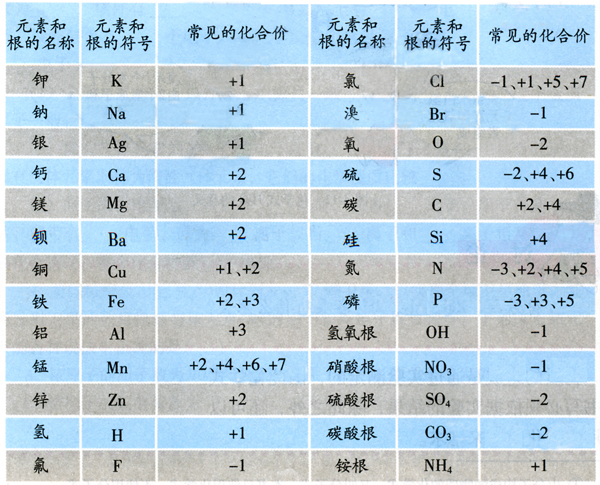
在化合物里,正负化合价的代数和为零,在单质分子里,元素的化合价为零。根据元素的化合价可以正确写出物质的化学式。
常见元素化合价的顺口溜之一: 氟氯溴碘钾钠银
铍镁钙锶钡和锌
硼铝为三硅为四
铜铁可变要记清。
铍镁钙锶钡和锌
硼铝为三硅为四
铜铁可变要记清。
常见元素化合价的顺口溜之二:一价钾、钠、氯、氢、银
二价氧、钙、钡、镁、锌
二、三铁,二、四碳
二、四、六硫要记全
二价氧、钙、钡、镁、锌
二、三铁,二、四碳
二、四、六硫要记全
②在写1价离子式时,习惯上要省略1,如钠离子是Na+、氯离子是Cl-,但不能写成Na1+,Cl1-;
③标出化学式里各离子所带电荷数时,若电荷数是1,则1应省略。
在标明元素的化合价时,若是+1价或-1价,1不能省略。如标出食盐和水里各元素的化合价应是
| 学有所用 |  |
元素组合中的化合价
一个分子式告诉我们两件事:一个原子的种类;一是这些原子在化合物中的数目。例如,氯化钙(CaCl2)这个分子式告诉我们:它由两种原子――钙和氯组成,而且是一个钙原子和二个氯原子结合起来的。
如果把金属钠放到盛有氯气的容器里,并且加热,那么,容器里就会有氯化钠反应,产物总是氯化钠(NaCl),而氯和镁反应生成的总是氯化镁(MgCl2)。我们把一个原子能和其他原子相结合的数目,称作它的“化合价”(原子价)。化合价的单位是以氢原子的化合价为标准,由于一个氢原子最多只能跟其他元素一个原子化合,所以是一价。
元素的化合价还呈现正负性。我们规定氢为 +1 价,那么,能与之结合的其他元素的化合价呈负价。由于一个氯原子只能与一个氢原子结合,所以氯呈-1价。依此类推,钠呈+1价,铁呈+3价。
化合价 === 氧的化合价×氧原子数。弄清了这个关系,就可以根据元素的化合价来写化合物的分子式了。例如,已经知道氧是-2价,铝是+3价,要写出氧化铝的分子式Al2O3,就比较容易了。还有这样一个规则:甲、乙两种元素化合而成的化合物里,甲元素的化合价总数必然和乙元素的化合价总数相等。以P2O5(五氧化二磷)为例,在这个分子里,磷的化合价×磷原子数 === 氧的化合价×氧原子数
| 沙场练兵 |  |
1. 下列说法正确的是( )
A.元素的化合价数值等于一个原子得失电子的数目
B.铁的化合价为零
C.水中氢气的化合价为零
D.单质铜中铜元素化合价为零,化合物中铜元素化合价为+1或+2价
2. 下列关于元素化合价的叙述,正确的是( )
A.元素化合价是一种元素一定数目的原子跟其他元素一定数目的原子化合的性质
B.在离子化合物里元素的化合价的数值,就是这种元素的原子得到或失去电子的数目
C.在共价化合物里,元素化合价的数值就是这种元素的一个原子跟其他元素的原子形成共用电子对的数目
D.在化合物中,金属元素显负价
E.一种元素的化合价,是一个固定不变的数值。因此,一种元素只能有一种化合价
3. 核电荷数为下列数值的各元素,能形成X2Y型化合物的是( )
A.14和10 B.6和8 C.11和8 D.12和16
4. 下列符号中,可以表示镁元素为+2价的是( )
A.Mg+2 B.
![]() C.
C.
![]() D.Mg2+
D.Mg2+
5. 下列关于化合价的说法中,正确的是( )
A.H2中H的化合价为+1价
B.H2O中氧元素的化合价为-2价
C.一种元素只有一种化合价
D.非金属元素在跟其它元素化合时,一定显负价
6. 下列有关化合价的说法中正确的是( )
A.在NaCl和HCl里,都是氯元素的1个原子得到1个电子,所以氯元素均为-1价
B.在H2中,氢元素显+1价
C.一种元素在同一种化合物里,可能显不同的化合价
D. 非金属元素在化合物里一定显负价
7. A元素的原子最外层上有6个电子,B元素的原子最外层上有3个电子,则A与B所形成化合物的化学式为( )
A.
AB2 B. A2B
C.
B2A3 D.
B3A2