5.复习时,要有意勤思多虑进行一题多解的训练
对同一道题,由于对题目的理解角度不同,解题的思路和方法也就会有所不同,但都可以取得相同的结果,这可称为一题多解。进行一题多解的训练,不仅能够选择最简捷的方法求解,还能开拓思路,提高解题技巧和能力,同时有助于对化学知识的理解和运用,有助于培养思维能力。
【例4】某碳酸钠溶液质量为12克,加入50克盐酸溶液恰好完全反应,已知盐酸溶液中溶质的质量分数为14.6%。求反应后溶液中溶质的质量分数。
解1:设反应生成的氯化钠质量为x,水的质量为y,参加反应的碳酸钠的质量为z。
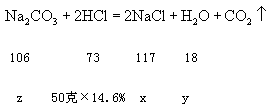
![]()
![]()
![]()
![]()
![]()
![]()
碳酸钠溶液含水的质量=12克-10.6克=1.4克
盐酸溶液含水的质量=50克×(1-14.6%)=42.7克
反应后氯化钠溶液质量![]()
氯化钠溶液中的溶质的质量分数![]()
答:反应后溶液中溶质的质量分数为20.3%。
解2:设反应生成的氯化钠质量为x,二氧化碳质量为y。

![]()
![]()
![]()
![]()
反应后氯化钠溶液的质量=12克+50克-4.4克=57.6克
氯化钠溶液中溶质的质量分数![]()
答:略。
以上两种解法的主要区别是求反应后溶液中溶质的质量分数时,求溶液质量的方法不同。解法1是根据溶质质量+溶剂(水)质量=溶液质量,求出溶质(即生成的![]() )质量后,再求反应后溶液中水的质量。反应后溶液中水的质量不仅包括反应生成水的质量,还包括两种参加反应的溶液中原来含有的水的质量。因此要先求出参加反应的
)质量后,再求反应后溶液中水的质量。反应后溶液中水的质量不仅包括反应生成水的质量,还包括两种参加反应的溶液中原来含有的水的质量。因此要先求出参加反应的![]() 的质量,再求出碳酸钠溶液中水的质量,然后求出盐酸溶液中水的质量,及反应生成水的质量,用三份水的质量和溶质
的质量,再求出碳酸钠溶液中水的质量,然后求出盐酸溶液中水的质量,及反应生成水的质量,用三份水的质量和溶质![]() 的质量列式求反应后氯化钠溶液的质量,再求氯化钠溶液中溶质的质量分数。解法2是根据化学反应所遵循的质量守恒定律来求解的。根据质量守恒定律可推出:碳酸钠溶液质量+盐酸溶液质量=氯化钠溶液质量+二氧化碳气体质量,所以,氯化钠溶液质量=碳酸钠溶液质量+盐酸溶液质量-二氧化碳气体质量。因此要先求出二氧化碳气体的质量,再用题目已知的碳酸钠溶液和盐酸溶液的质量,及二氧化碳的质量,求出氯化钠溶液的质量,再求氯化钠溶液中溶质的质量分数。
的质量列式求反应后氯化钠溶液的质量,再求氯化钠溶液中溶质的质量分数。解法2是根据化学反应所遵循的质量守恒定律来求解的。根据质量守恒定律可推出:碳酸钠溶液质量+盐酸溶液质量=氯化钠溶液质量+二氧化碳气体质量,所以,氯化钠溶液质量=碳酸钠溶液质量+盐酸溶液质量-二氧化碳气体质量。因此要先求出二氧化碳气体的质量,再用题目已知的碳酸钠溶液和盐酸溶液的质量,及二氧化碳的质量,求出氯化钠溶液的质量,再求氯化钠溶液中溶质的质量分数。
从上面两种解法看,解法2比解法1简便,说明在有关化学方程式的化学计算题中,运用质量守恒定律解题是一种较好的解题方法。